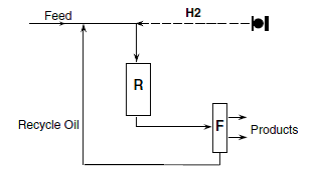
Reaksi Hydrocracking
Reaksi hydrocracking mengubah umpan fraksi berat menjadi
produk dengan berat molekul yang lebih ringan dengan disertai penghilangan sulfur dan nitrogen serta
penjenuhan senyawa olefin dan aromatik. Sulfur organik diubah menjadi senyawa H2S
sedangkan senyawa nitrogen diubah menjadi NH3 dan senyawa oksigen
(tidak selalu ada) diubah menjadi H2O. Reaksi pada hydrocracking
dapat dikelompokkan menjadi dua kategori: reaksi yang diharapkan dan reaksi
yang tidak diharapkan.
Reaksi yang diharapkan di sini meliputi treating,
penjenuhan, dan reaksi cracking. Reaksi yang tidak diharapkan adalah terjadinya
keracunan katalisator oleh kontaminan (impurities) dalam bentuk reaksi coking
pada katalisator.
Terdapat dua tipe reaksi yang terjadi pada unit
hydrocracking, yakni treating (disebut juga pre-treating) dan cracking (disebut
juga hydrocracking). Reaksi cracking membutuhkan katalis dual fungsi
(bi-functional catalyst) yang mengkatalisis dua jenis reaksi, yakni cracking
dan hidrogenasi (penjenuhan).
Reaksi Treating
Reaksi treating yang terjadi pada unit hydrocracking antara
lain reaksi penghilangan sulfur, nitrogen, senyawa organo-metallic, oksigen,
dan juga senyawa halida. Senyawa sulfur, nitrogen, dan oksigen merupakan tiga
senyawa yang selalu ada dalam umpan unit hydrocracking. Kadarnya beragam,
tergantung pada sumber dan jenis feedstock. Senyawa lainnya tidak selalu ada
dalam umpan unit hydrocracking.
Secara umum, konsumsi hidrogen untuk reaksi treating dapat
dilihat pada tabel berikut ini.
Reaksi hidrodesulfurisasi terjadi dengan penghilangan sulfur
yang diikuti dengan reaksi penjenuhan senyawa olefin yang terbentuk. Berikut ini
adalah contoh reaksi hidrodesulfurisasi.
Reaksi denitrogenasi terjadi dengan pola yang berbeda.
Mekasnisme hidrodenitrogenasi bermula dengan reaksi penjenuhan aromatik diikuti
dengan hidrogenolisis dan diakhiri dengan denitrogenasi. Berikut ini adalah
contoh beberapa mekanisme hidrodenitrogenasi.
Reaksi Cracking
Reaksi hydrocracking berlangsung dengan mekanisme
bi-functional. Mekanisme bi-functional membutuhkan dua tipe sisi katalis yang
berbeda guna mengkatalisis tahapan reaksi yang terpisah dalam suatu rangkaian
reaksi. Dua fungsi yang dimaksud adalah fungsi asam yang mengkatalisis reaksi
cracking dan isomerisasi serta fungsi logam yang mengkatalisis reaksi
pembentukan olefin dan hidrogenasi. Reaksi cracking membutuhkan panas sedangkan
reaksi hidrogenasi menghasilkan panas. Secara keseluruhan, reaksi hydrocracking
menghasilkan panas. Sebagaimana pada reaksi treating, reaksi hydrocracking juga
merupakan fungsi dari konsumsi hidrogen, artinya semakin banyak konsumsi
hidrogen, maka akan semakin eksotermis reaksi yang terjadi.
Konsumsi hidrogen pada reaksi hydrocracking secara umum
(termasuk pre-treating) adalah 1200 - 2400 SCFB/wt% dengan perubahan sebesar
200 – 420 Nm3/m3 tiap %wt perubahan kapasitas umpan.
Panas yang dihasilkan dari reaksi antara 50 – 100 Btu/SCF H2 atau
jika dinyatakan dalam kenaikan temperatur adalah sebesar 0,065oF/SCF
hidrogen yang dikonsumsi (0,006oC/Nm3/m3 H2).
Secara umum, reaksi hydrocracking dimulai dengan pembentukan
olefin atau siklo-olefin pada sisi logam katalis. Selanjutnya sisi asam akan
menambahkan proton pada olefin atau siklo-olefin tersebut untuk menghasilkan
ion carbonium. Ion carbonium tersebut akan terrengkah menjadi ion carbonium
yang lebih kecil dan senyawa olefin yang lebih kecil. Produk tersebut merupakan
produk utama hydrocracking. Proses terminasi pada reaksi hydrocracking terjadi
dengan reaksi penjenuhan senyawa olefin pada sisi logam katalisator. Berikut ini
adalah tahapan reaksi pada rangkaian reaksi hydrocracking terhadap suatu
senyawa n-parafin.
Dari reaksi tersebut dapat diketahui bahwa pada awal reaksi
hydrocracking terbentuk senyawa olefin yang dikatalisis oleh sisi logam. Kemudian
olefin tersebut diubah menjadi ion carbonium. Ion carbonium tersebut terisomerisasi
menjadi ion carbonium tersier yang lebih stabil. Selanjutnya terjadi
perengkahan ion carbonium tersebut pada ikatan pada posisi β
terhadap muatan ion carbonium tersebut. Posisi β merupakan ikatan kedua dari muatan
ion. Ion carbonium dapat bereaksi dengan olefin untuk mentransferkan muatan
dari satu fragmen ke fragmen lainnya. Dengan cara ini muatan dapat ditransfer
dari senyawa hidrokarbon rantai pendek ke senyawa hidrokarbon rantai lebih
panjang yang dapat mengakomodasi muatan dengan lebih baik. Akhirnya, reaksi
penjenuhan terhadap olefin terjadi pada sisi logam katalisator.
Reaksi hydrocracking merupakan reaksi yang selektif terhadap
parafin dengan jumlah atom karbon yang banyak. Hal ini terjadi dalam rangka
mencapai kesetimbangan untuk membentuk olefin dengan jumlah atom karbon yang
banyak. Di samping itu, parafin dengan jumlah atom karbon lebih banyak dapat
mengadsorb lebih kuat. Ion carbonium intermedia menyebabkan isomerisasi yang
berlebih pada produk reaksi khususnya pada α-metil isomer. Hal ini karena
ion carbonium tersier lebih stabil. Oleh karena itu, produksi C1 dan
C3 rendah karena produksi gas hidrokarbon tersebut terjadi ketika
terbentuknya ion carbonium primer dan sekunder yang sebenarnya kurang
dikehendaki. Senyawa-senyawa lain seperti alkil-naften, alkil-aromat, dan lain
sebagainya bereaksi dengan mekanisme serupa melalui reaksi pembentukan ion
carbonium.
Berikut ini adalah data termodinamika dari beberapa reaksi
utama pada proses hydrocracking.
Referensi:
David S. J. “Stan” Jones and Peter R. Pujado, 2006, Handbook
of Petroleum Processing, Netherland: Springer













 20.51
20.51
 fromesa
fromesa